Natura imitatzen ingurumen berde eta osasungarri bat ahalbidetzeko
Edozein izakik bizirauteko aukera gehiago izango ditu bere buruarentzat, nolabait errentagarria den moduan pixka bat aldatzen bada… eta, beraz, modu naturalean hautatua izango da. Herentziaren printzipio sendotik abiatuta, hautatutako barietate orok forma berria eta eraldatua hedatzeko joera izango du”.
Charles Robert Darwin (1809-1882), Espezieen jatorria.
Industria aroa hasi zenetik, jarduera antropogenikoek etengabe eraldatu dituzte ekosistemak. XX. eta XXI. mendeetan lortutako aurrerapen teknologikoak eta kutsaduraren hazkundea txanpon beraren bi aldeak dira. Nahiz eta naturak beti aurkitu dituen ingurumen-desorekak arintzeko modu adimentsu eta sofistikatuak, substantzia kaltegarrien ekoizpen- eta askapen-tasa ez dator bat biomakinariaren autoegokitzapen-ahalmenarekin. Hori dela eta, berotegi-efektuko gasen metaketak eta kutsatzaile iraunkorrek atmosferaren, lurzoruaren eta uraren zikloen oreka aldatu dute. Ingurumen ez-toxiko bat lortu ahal izateko, kaltegarriak diren substantziak ezabatzeaz gain, bioerregaiak ekologikoki ekoiztu behar dira, giza jardueren karbono-aztarna murrizteko.
Ingurumen-kutsadurari aurre egiteko, naturak kaltegarriak diren substantzia kimiko eta gasak harrapatu eta biologikoki erabilgarriak diren substantzia bihurtzen ditu. Funtzio hau betetzeko gai diren bio-makina konplexuen artean, entzimak, eta bereziki, metaloentzimak dira nagusi.3,4 Nahiz eta bioingeniariek entzimak eta metaloentzimak aplikazio industrialetan erabili ahal izateko egokitu dituzten, biosistema hauek eragozpen nabarmen bat dute: bizitza posible den inguruetatik kanpo funtzionatzeko behar den egonkortasun kimiko eta termiko falta. Honen arrazoi nagusia da entzimen eta proteinen egitura tridimentsional eder eta konplexuak elkarrekintza ahulez osatuak daudela eta baldintza kimiko eta termiko gogorretan hautsi egiten direla.
Entzimak aminoazido-kate luzeen tolesturatik sortzen diren hiru dimentsioko egitura konplexuak dira (1a-c irudia). Entzimen aldamio malgu eta dinamikoen forma aminoazido-hondakinek peptido-sekuentzien barruan ezartzen dituzten elkarrekintza ahulen ondorioa da nagusiki (1d irudia). Elkarrekintza hauez gain, egitura tridimentsionala ur-molekulei, talde protesikoei eta entzimaren barruan dauden kofaktoreei esker egonkortzen da, haiek zeregin estruktural eta funtzional kritikoak betetzen dituztelarik (1e irudia).
Entzimek giltza-blokeo mekanismoaren bidez banakako molekulak ezagutu eta eraldatzeko gai diren poltsiko aktibo sofistikatuak dituzte. Metaloproteinen kasuan, poltsa aktiboak entzimaren aldamioan dauden aminoazido hondakinekin koordinatzen diren ioi metaliko indibidualak edo taldekatuak jasotzen ditu. Oro har, egitura konplexu horien barruan dauden bio-metalek koordinazio-esfera zurrunak dituzte, eta esfera horiek espezie labilez osatuak daude gehienetan (hau da, ura edo aminoazido lotura-taldeak). Talde koordinatzaile labilak atera ondoren, aktibatu egiten da metaloentzimaren nukleoa, oso erreaktiboak diren leku katalitiko irekiak (1e irudia).6
Baina metalaren lehen koordinazio-esfera ez da axola duen bakarra. Bigarren sasi-koordinazio distantzietara dauden aminoazido hondakinen taldeen kokapen eta antolaketa espezifikoak bio-metalen jarduera katalitikoa modulatzen du, metalen propietate elektronikoak eta erredox propietateetan eragiten baitu. Aldi berean, bigarren geruza honek metalaren nukleoa inguratzen duen poltsiko entzimatikoaren eremu elektrikoa eta izaera hidrofobiko/hidrofilikoa modulatzen ditu. Poltsikoaren gainazalaren dekorazioa eta egitura orokorraren plastikotasuna konbinatzeak poltsikoaren forma eta funtzioa espezifikoki egokitzen laguntzen du, substratuak ezagutu, aktibatu eta eraldatzeko (1e irudia).7
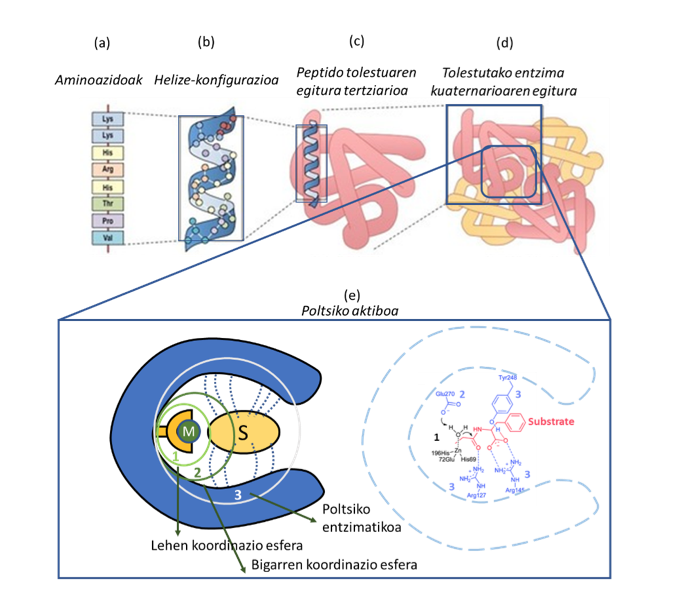
Entzimak eta metaloentzimak sei talde nagusitan sailkatzen dira banakako funtzionalitatearen arabera:
- oxidorreduktasak (Fe, Cu eta Mo ioiak),
- transferasak (Mg, Mn eta Co metalak),
- hidrolasak (Ca, Zn, Co, Mn eta Mg ioiak),
- liasak (batez ere Ca, Mg, Mn, Cn, Co eta Zn), isomerasak (Mn, Co and Fe biometalak) eta
- ligasak (Mg eta Mn ioiak) (2. irudia).
Entzimek fotosintesia eta ioi/elektroien garraio eta erregulazioa bezalako prozesu eder eta sofistikatuetan parte hartzen dute. Hauek jarduera entzimatikoa katean eta modu itzulgarrian behar duten adibide pare bat baino ez dira, non jarduera entzimatiko baten irteerak (hau da, argia, elektroiak, molekula organikoen protoiak) hurrengoaren sarrera elikatzen duen.8
Metaloproteinen biokimika hedatzeko, ikerketa-ahalegin handiak egin dira, entzimak irekitzen diren baldintza zehatzetatik kanpo funtzionatzeko gai diren sistema sendoak lortzeko asmoarekin. Alde batetik, biokimikariek entzimen aplikazio esparrua industria- eta ingurumen-helburuetarako zabaltzea lortu dute, baina entzimen egonkortasuna tenperatura, azidotasuna eta disolbatzaile-baldintza leunetara mugatzen da.9 Gainera, aldamio sendoetan entzimak eta metaloentzimak immobilizatu eta/edo kapsulatzeko aukerak ireki egin du epe luzerako egonkortasuna hobetzeko ikuspegia .10 Bestalde, ikertzaile askok koordinazio-konposatuetan oinarritutako katalizatzaile homogeneoen muntaketa aztertu dute, katalizatzaile hauek entzimen antzeko nukleo metalikoa baitute. Dena den, koordinazio-konposatu hauek entzimen antzeko mugak dituzte. Hirugarrenik, ikertzaileek metaloentzimen nukleo aktiboak euskarri polimeriko, biopolimeriko eta ez-organiko askotan erreplikatzen saiatu dira, nahiz eta bio-metalen bigarren koordinazio-geruzaren eta poltsiko katalitikoaren forma eta kimikaren gaineko kontrola edukitzea erronka handia den.11
Honetara heldurik galdera bat sortzen da: ikertzaileek metaloentzimen funtzioak imitatzeaz gain haien egonkortasuna hobetu dezakete, beren espezifikotasuna eta eraginkortasuna elkarrekintza ahulez egonkortutako egitura tridimentsional malguetan oinarritzen bada?
Hemen sartzen dira jokoan sare metalorganikoak (Metal Organic Framework, MOF). MOFak zubi kobalente indartsuen bidez lotuta dauden kluster metaliko eta estekatzaile organikoz osatutako material porotsu eta ordenatuak dira.12 Kluster metaliko eta estekatzaileen geometria, luzera eta konektibitatea aldatuz, MOFek metaloentzimen jarduera imitatzeko behar duten topologia, porositatea eta izaera kimikoa izatea lor daiteke. Adibidez, orain arte kimika erretikularrak ondorengoak ahalbidetu ditu:
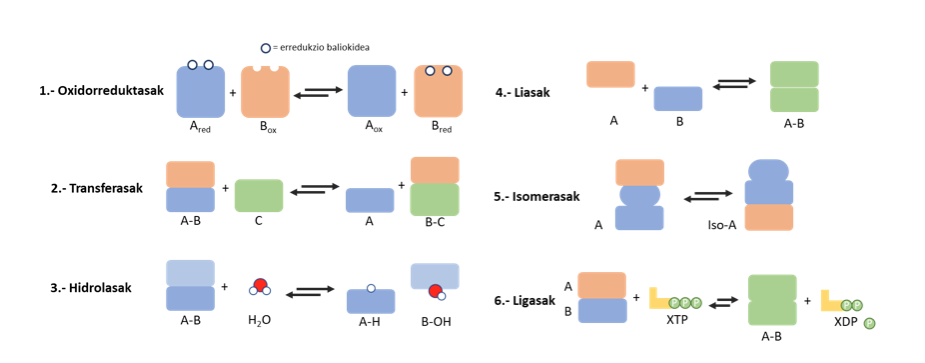
- bio-metalak eta/edo talde bio-organikoetatik (hau da, peptidoak, aminoazidoak, porfirinak…) abiatuz metaloentzima jakin batzuen poltsiko eta/edo talde protesikoak imitatzen dituzten MOFak eraikitzea,13
- sarean ioi metalikoak trukatu edo eranstea, metaloentzimen poltsikoetako metal-ligando loturak imitatzeko eta
- aminoazido-hondakin funtzionalak gehitzea metaloentzima artifizialen funtzioa areagotzeko (3. irudia).14
Gainera, nahiz eta sare tinkoak izan, MOF batzuek porositatea eta poroen irekiera birmoldatu dezakete poroetan dituzten molekulen arabera. Entzimen aldamio tridimentsional malguek bezala, MOF batzuek molekulak ezagutu ondoren beraien sareak distortsionatu eta berregokitu ditzakete.15 Etapa honetan, MOF sisteman metaloentzimen inguruan egin diren ikerketa gehienak biokatalizatzaileetan dauden gune metaliko antzekoen sintesi edo instalazioan oinarritu dira. Halaber, zenbait ahalegin egin dira MOFen barruan dauden ioi metalikoen koordinazio-inguruak moldatzeko. Ikerketa-ikuspegi honen hastapenetan gauden arren, hasierako emaitzak benetan oparoak dira, eta horrek sistema horiek erregai berdeak ekoizteko eta ingurumena hobetzeko duten ahalmena erakusten du. Orain arte MOF-metaloentzima sistemak hiru aplikazio-eremu nagusitan ebaluatu izan ohi dira:
- Deskarbonizazio globala anhidrasaren antzeko jarduera bientzimatikoaren bidez: karbono dioxidoa harrapatu eta karbonato bihurtu (III motako hidrolasa jarduera).
- Erregai berdeen ekoizpena monooxigenasa eta hidrogenasa motako entzimak imitatuz: protoien murrizketa hidrogenoa sortzeko / alkanoen oxidazio katalitikoa (I motako oxidorreduktasa jarduera entzimatikoa).
- Produktu kimiko arriskutsuen oxidazioa eta inaktibazioa, hala nola fenolak, pestizidak eta gerrako agenteak (I motako oxidorreduktasa eta III motako hidrolasa jarduerak).
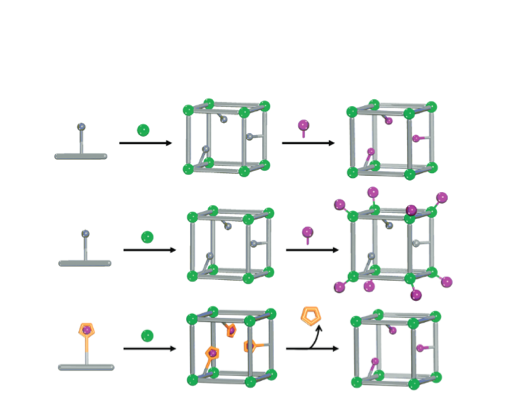
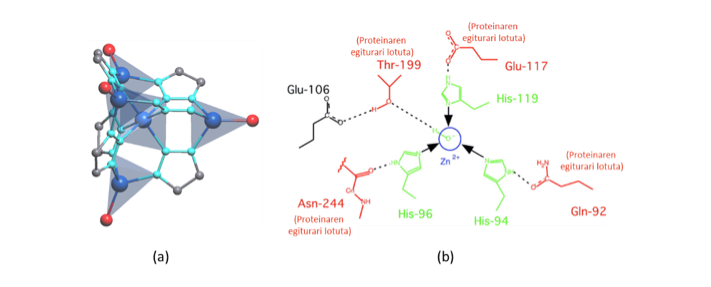
Karbono dioxidoa harrapatzeko eta eraldatzeko aktibitate entzimatikoa duen MOF baten adibide nabarmen bat M. Dincă-k eta lankideek argitaratu zuten.16 Anhidrasa karbonikoaren antzeko jarduera duen MOF bat diseinatzeko asmoz, MFU-4l MOF ezagunaren metal nodoak arrazionalki aldatu zituzten (N3Zn‒Cl unitate terminalak N3Zn‒OH unitateetan bilakatu zituzten, 4. irudia). Honela MOFak anhidrasa karbonikoarekin eta antzeko entzimekin duen antza handitzea lortu zuten, karbono dioxidoaren hidratazioa eta deshidratazioa katalizatzeko (H2O + CO2 ↔ HCO3‒ + H+). Material berriak CO2 kantitate handiak modu itzulgarrian harrapatzen ditu (N3Zn‒OH ↔ N3Zn‒OCOOH), eta paraleloki aktiboa da, 4-nitrofenil azetatoaren hidrolisirako, anhidrasa karbonikoaren jarduera imitatzen duenez gero. Harrapatze-ahalmen esanguratsua (3.41 mmol g-1 298 K-tara) eta birsortzeko behar duen energia-kostu baxua kontsideratuz gero, material honek CO2 harrapatu eta bahitzeko aukera handia eskaintzen du.
Eskisto-gasaren konbertsio deszentralizatua lortzeko gakoetako bat da alkanoak erraz kondentsatu daitezkeen oxigenodun energia garraiatzaileak (metanola, etanola) bihurtzea. Metanoa oso tenperatura altuetan metanol bihur daitekeen arren, giro tenperaturan gertatzen den metanoaren zuzeneko oxidazioa metaloentzimen kontua da.
Halaber, alkanoak tenperatura baxuetan metaloentzima motako MOFen bidez oxidatu daitezkeela frogatu da. Burdin oxidasetan aurkitzen diren metal-oxo zatien antzeko metalklusterdun MOFak erabiliz. D. J. Xiao-k eta lankideek frogatu etin zuten Fe2(dobdc) MOFaren espin altuko Fe ioiek etanoa etanol bilakatu dezaketela. Fe2(dobdc) MOFaren burdinezko gune metaliko irekiek N2O aktibatzen dute, etanoaren oxidazioa bultzatzen dute.17
Era berean, zirkonioan oinarritutako MOF mikro- eta mesoporotsu asko matrize gisa erabili dira 85 °C-ra metano monooxigenasaren antzeko aktibitatea duten kobre eta burdinan oinarritutako espezie monomeriko, dimeriko eta trimerikoak instalatzeko. 18,19
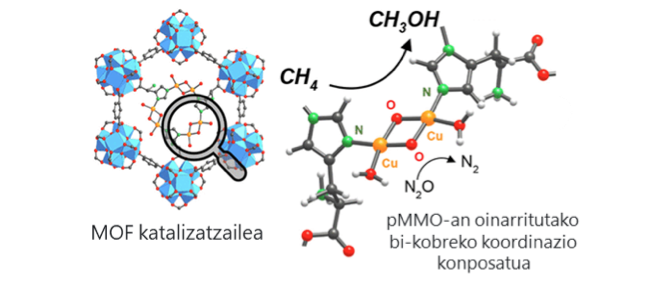
Pauso bat aurrerago joanez, J. Bae-k eta lankideek kobre unitate dimerikoei koordinatutako histidina-hondakinak instalatu zituzten zirkonio trimesato MOF-808an (5. irudia). Kobreak metano monooxigenasaren antzeko antolaketa duelarik, material honek orain arte ikusi den metanolaren produktibitate eta selektibitaterik handiena erakutsi zuen (71,8 µmol/g) 150 °C-ko tratamendu isotermikoetan.20
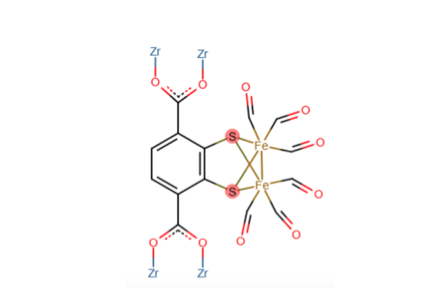
Argia erregai bihurtzeko asmoz, Fe-Fe konplexu binuklearrak zirkoniozko MOF matrizeetan ere finkatu dira hidrogenoaren ekoizpen berderako. Hidrogenasa motako FeFe gunea UiO-66 zirkonio tereftalatozko MOF egitura porotsuaren barruan egonkortu da, protoien hidrogenorako erredukzio elektro eta fotokimikoa bideratuz (6. irudia).21 Hidrogenasa motako MOFen egonkortasun eta errendimendu katalitikoak FeFe katalizatzaile homogeneoena gainditzen du, eta horrek frogatu egiten ditu zentro katalitiko aktiboak MOF bidez babesteak dituen onurak.
Laburbilduz, kimika erretikularrak egitura kimiko eta termiko egonkorrak ematen ditu, non biokatalizatzaile metalikoen nukleoak erreplikatu eta instalatu daitezkeen. Oro har, metaloentzima moduko sare-sistemek etorkizun handia dute biokatalizatzaileen dibertsitatea eta esparru operatiboa zabaltzeko. Hala ere, garrantzitsua da aipatzea orain arte sei funtzio entzimatiko nagusietatik bi bakarrik erreplikatu direla MOF metaloentzimetan: oxidorreduktasa eta hidrolasa jarduerak. Orain arte, transferasa, liasa, isomerasa edo ligasen jarduerak erakusten dituzten MOF bio-metalokatalizatzaileak esploratu gabe daude, nahiz eta katalisi asimetrikoan eta bereizketa enantiomerikoan erabiltzen diren MOF kiralek etorkizun handia duten aktibitate entzimatikoa imitatzen duen kimika erretikularraren potentziala hedatzeko.
Sistema entzimatikoak imitatzeko kimika erretikularra erabiltzearen perspektiba bere hastapenetan dago. Oraindik MOFen antzeko metaloentzima-sistemak hobetzeko aukera asko daude: entzimetako metalen biokoordinazio-nukleoak doitasunez diseinatzeko aukeraz gain, haien bigarren koordinazio-geruza eta inguruko poltsikoa kluster eta estekatzaileen aldagai anitzeko kodifikazioren bidez doitzeko aukera ere badago. Propietate anisotropikoak dituzten poro asimetrikoen diseinu arrazionala (hau da, eremu elektrikoa, izaera hidrofiloa/hidrofoboa…) funtsezko mugarria izango da entzimek banakako substratuak ezagutzeko duten espezifikotasun handiari heltzeko. MOFen ohiko sintesi aurreko edo osteko funtzionalizazio-kimikatik urrun, inprimaketa molekularrak ahalmen handia izan lezake aminoazido-hondakinen kokapen espezifikoa eta disposizioa MOFen espazio porotsuan kontrolatzeko. Aldi berean, MOF malguen portaera dinamikoaz balia gaitezke metaloentzima erretikularrez osatutako materialak substratu espezifikoak hartzeko gai diren sare automoldagarriez hornitzeko. Halako sareen aktibazioa poltsiko aktiboa erreplikatu den sare porotsua distortsionatu edo tenkatzen duten kanpo estimuluen bidez lortu daiteke.
Harrigarria izango da, metaloentzima erretikularren kimikaren oinarriak finkatu ondoren, sistema entzimatikoak garatzeko erabiltzen den eboluzio zuzeneko ikuspegia sare organometalikoetan ere aplika ote daitekeen ikustea. Aurrerapauso bat emanez, sistemek eraginkortasun berdinez transferitu eta transforma ditzakete kate-prozesuetan parte hartzen duten produktu katalitikoak. Beraz, arestian aipatutako helburuak erronka handiak badira ere, liluragarria izango da metaloentzimez osatutako MOFen aktibitate biokatalitikoa kate-erreakzioetan akoplatu ote daitekeen ikustea.
Erreferentzia bibliografikoak:
- Heux, S.; Meynial-Salles, I.; O’Donohue, M. J.; Dumon, C. (2015). White Biotechnology: State of the Art Strategies for the Development of Biocatalysts for Biorefining. Biotechnology Advances, 33 (8), 1653–1670. DOI: 10.1016/j.biotechadv.2015.08.004
- Commision, E. The European Green Deal (2019). Communication from the commision from the commision to the European Parliament, The European Council, The Council, the European Economic and Social Commitee and the Comittee of the regions.
- Desage-El Murr, M. (2020). Nature Is the Cure: Engineering Natural Redox Cofactors for Biomimetic and Bioinspired Catalysis. ChemCatChem, 12 (1), 53–62. DOI: https://doi.org/10.1002/cctc.201901642
- Zastrow, M. L.; Pecoraro, V. L. (2013). Designing Functional Metalloproteins: From Structural to Catalytic Metal. Sites. Coordination Chemistry Reviews, 257 (17–18), 2565–2588. DOI: https://doi.org/10.1016/j.ccr.2013.02.007
- Fontecilla-Camps, J. C.; Amara, P.; Cavazza, C.; Nicolet, Y.; Volbeda, A. (2009). Structure-Function Relationships of Anaerobic Gas-Processing Metalloenzymes. Nature, 460 (7257), 814–822. DOI: https://doi.org/10.1038/nature08299
- Moura, I.; Pauleta, S. R.; Moura, J. J. G. (2008). Enzymatic Activity Mastered by Altering Metal Coordination Spheres. Journal of Biological Inorganic Chemistry, 13 (8), 1185–1195. DOI: https://doi.org/10.1007/s00775-008-0414-3
- Ji, Z.; Wang, H.; Canossa, S.; Wuttke, S.; Yaghi, O. M. (2020). Pore Chemistry of Metal–Organic Frameworks. Advanced Functional Materials, 30 (41), 2000238. DOI: https://doi.org/10.1002/adfm.202000238
- Waldron, K. J.; Rutherford, J. C.; Ford, D.; Robinson, N. J. (2009). Metalloproteins and Metal Sensing. Nature, 460 (7257), 823–830. DOI: https://doi.org/10.1038/nature08300
- Thompson, Z.; Cowan, J. A. (2020). Artificial Metalloenzymes: Recent Developments and Innovations in Bioinorganic Catalysis. Nano Micro Small, 16 (27), 2000392. DOI: https://doi.org/10.1002/smll.202000392
- Wei, T. H.; Wu, S. H.; Huang, Y. Da; Lo, W. S.; Williams, B. P.; Chen, S. Y.; Yang, H. C.; Hsu, Y. S.; Lin, Z. Y.; Chen, X. H.; Kuo, P. E.; Chou, L. Y.; Tsung, C. K.; Shieh, F. K. (2019). Rapid Mechanochemical Encapsulation of Biocatalysts into Robust Metal–Organic Frameworks. Nature Communications, 10 (1), 1–8. DOI: https://doi.org/10.1038/s41467-019-12966-0
- Davis, H. J.; Ward, T. R. (2019). Artificial Metalloenzymes: Challenges and Opportunities. ACS Central Science, 5 (7), 1120–1136. DOI: https://doi.org/10.1021/acscentsci.9b00397
- Freund, R.; Canossa, S.; Cohen, S. M.; Yan, W.; Deng, H.; Guillerm, V.; Eddaoudi, M.; Madden, D. G.; Fairen-Jimenez, D.; Lyu, H.; Macreadie, L. K.; Ji, Z.; Zhang, Y.; Wang, B.; Haase, F.; Wöll, C.; Zaremba, O.; Andreo, J.; Wuttke, S.; Diercks, C. S. (2021). 25 Years of Reticular Chemistry. Angewandte Chemie International Edition.
- Peng, J.; Wu, R. (2018). Metal–Organic Frameworks in Proteomics/Peptidomics-A Review. Analytica Chimica Acta, 1027, 9–21. DOI: https://doi.org/10.1016/j.aca.2018.04.069
- Cohen, S. M. (2012). Postsynthetic Methods for the Functionalization of Metal-Organic Frameworks. Chemical Reviews, 112 (2), 970–1000. DOI: https://doi.org/10.1021/cr200179u
- Serre, C.; Devic, T. (2016). Iron and Groups V- and VI-Based MOFs. The Chemistry of Metal–Organic Frameworks: Synthesis, Characterization, and Applications, 171–202. DOI:10.1002/9783527693078.ch7
- Sun, Q.; Aguila, B.; Ma, S. (2018). Metalloenzyme Mimicry at the Nodes of Metal-Organic Frameworks. Chem, 4 (12), 2736–2738. DOI:10.1016/j.chempr.2018.11.017
- Xiao, D. J.; Bloch, E. D.; Mason, J. A.; Queen, W. L.; Hudson, M. R.; Planas, N.; Borycz, J.; Dzubak, A. L.; Verma, P.; Lee, K.; Bonino, F.; Crocellà, V.; Yano, J.; Bordiga, S.; Truhlar, D. G.; Gagliardi, L.; Brown, C. M.; Long, J. R. (2014). Oxidation of Ethane to Ethanol by N2 O in a Metal-Organic Framework with Coordinatively Unsaturated Iron(II) Sites. Nature Chemistry, 6 (7), 590–595. DOI: https://doi.org/10.1038/nchem.1956
- Ikuno, T.; Zheng, J.; Vjunov, A.; Sanchez-Sanchez, M.; Ortuño, M. A.; Pahls, D. R.; Fulton, J. L.; Camaioni, D. M.; Li, Z.; Ray, D.; Mehdi, B. L.; Browning, N. D.; Farha, O. K.; Hupp, J. T.; Cramer, C. J.; Gagliardi, L.; Lercher, J. A. (2017). Methane Oxidation to Methanol Catalyzed by Cu-Oxo Clusters Stabilized in NU-1000 Metal-Organic Framework. Journal of the American Chemical Society, 139 (30), 10294–10301. DOI: https://doi.org/10.1021/jacs.7b02936
- Zheng, J.; Ye, J.; Ortuño, M. A.; Fulton, J. L.; Gutiérrez, O. Y.; Camaioni, D. M.; Motkuri, R. K.; Li, Z.; Webber, T. E.; Mehdi, B. L.; Browning, N. D.; Penn, R. L.; Farha, O. K.; Hupp, J. T.; Truhlar, D. G.; Cramer, C. J.; Lercher, J. A. (2019). Selective Methane Oxidation to Methanol on Cu-Oxo Dimers Stabilized by Zirconia Nodes of an NU-1000 Metal-Organic Framework. Journal of the American Chemical Society, 141 (23), 9292–9304. DOI: https://doi.org/10.1021/jacs.9b02902
- Baek, J.; Rungtaweevoranit, B.; Pei, X.; Park, M.; Fakra, S. C.; Liu, Y. S.; Matheu, R.; Alshmimri, S. A.; Alshehri, S.; Trickett, C. A.; Somorjai, G. A.; Yaghi, O. M. (2018). Bioinspired Metal-Organic Framework Catalysts for Selective Methane Oxidation to Methanol. Journal of the American Chemical Society, 140 (51), 18208–18216. DOI: https://doi.org/10.1021/jacs.8b11525
- Pullen, S.; Fei, H.; Orthaber, A.; Cohen, S. M.; Ott, S. (2013). Enhanced Photochemical Hydrogen Production by a Molecular Diiron Catalyst Incorporated into a Metal-Organic Framework. Journal of the American Chemical Society, 135 (45), 16997–17003. DOI: https://doi.org/10.1021/ja407176p
- Wu, J.; Wang, Z.; Jin, X.; Zhang, S.; Li, T.; Zhang, Y.; Xing, H.; Yu, Y.; Zhang, H.; Gao, X.; Wei, H. (2021). Hammett Relationship in Oxidase-Mimicking Metal–Organic Frameworks Revealed through a Protein-Engineering-Inspired Strategy. Advanced Materials, 33 (3), 2005024. DOI: https://doi.org/10.1002/adma.202005024
- Gil-San-Millan, R.; López-Maya, E.; Platero-Prats, A. E.; Torres-Pérez, V.; Delgado, P.; Augustyniak, A. W.; Kim, M. K.; Lee, H. W.; Ryu, S. G.; Navarro, J. A. R. (2019). Magnesium Exchanged Zirconium Metal-Organic Frameworks with Improved Detoxification Properties of Nerve Agents. Journal of the American Chemical Society, 141 (30), 11801–11805. DOI: https://doi.org/10.1021/jacs.9b05571
Egileez:
Ainara Valverde eta Leire Celaya-Azcoaga, BCMaterials zentroko (@BCMaterials) eta EHUko Zientzia eta Teknologia Fakultateko ikertzaileak dira; Roberto Fernández de Luis BCMaterials zentroko ikertzailea da eta Itziar Oyarzabal, Ikerbasque ikertzailea da zentro berean.
1 iruzkina
[…] azala diseinatzeko gonbita helarazi zaie; azalean Alizia ageri da, ispilua zeharkatuz bere forma enantiomerikoa (ispilu-irudia) bihurtzeko zorian. Aliziak bidelagun bat aurkitzen du, katalizatzaile bat, azken […]