Masa-espektrometria (I). Neoi isotopoetatik elefante hegalariengana
Bilboko Zientzia Fakultatea, 1968/1969 ikasturtean jarri zen abian. Berrogeita hamar urte beranduago, Zientzia eta Teknologia Fakultateak ospatu egin nahi du urteurrena eta horretarako, gure Fakultate honek gizarteari ekarri dion onura goraipatzea baino gauza hobeagorik ez dago.
Beraz, bost hamarkada hauetan egindako ekarpenik garrantzitsuenak plazaratuko ditugu hurrengo asteetan, Cuaderno de Cultura Científica eta Zientzia Kaiera blogetan.
Hasiera emango diogu kontuari “masa-espektrometria” izeneko teknikaren berri emanez. Izan ere, oso adibide argigarria da Zientzia eta Teknika aurrera nora doazen ulertzeko unean.

J.J.Thomsonek XX. mendearen hasieran aztertu zituen eremu elektriko eta magnetikopeko ioien ibilbidearen aldaketa. Aurretik, 1906.eko Nobel Saria irabazia zuen, bere katodoko izpien ikerkuntzagatik. Izan ere, ordura arte ezezaguna zen elektroi izeneko partikula subatomikoa aurkitzeagatik. Ikerketa horretan aztertu zuen geroago aurretik aipatutako ibilbide-aldaketa. Sir Thomsonek, ikusi zuen masa/karga erlazioaren arabera banandu zitezkeela karga positiboko gasak, eta ezarritako eremu elektriko eta magnetikotik abiatuta ondo jakin zitekeela masa/karga erlazio hori. Beste era batera esanda, jakin zitekeen atomoen eta molekulen pisua zein ziren: Masa-espektrometria jaioa zen.
Egungo analisi-teknika moldakorrena eta ahaltsuena dugu masa-espektrometria. Izan ere, aukera ematen digu oso kantitate txikietan dauden konposatuen kontzentrazioa zehazteko, eta horretarako erabiltzen da hain zuzen ere analisi forentsean, edo elikagaien eta kutsatzaileen analisian. Gainera, molekula berriak identifikatzen ditu, eta horrek laguntza handia ematen du botika berrien sintesian. Areago, aurrerapen handiak eragiten ari da medikuntzan eta fisiologian, posible egiten baitu organo bitaletan molekula jakin batzuk nola banatzen diren jakitea. Artikulu sorta honetan zehar, aplikazio ugari hauen artetik ibiliko gara liluraturik. Hori egin baino lehen, ikus dezagun 100 bat urtean nola iritsi garen honelako egoerara.
Lehenengo urratsak
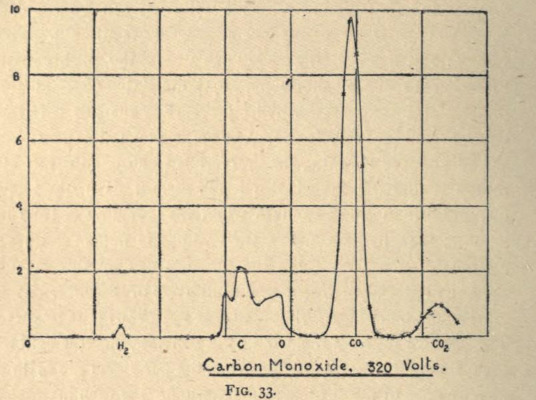
Goazen Cambridgeko Unibertsitatera, bertan Thomson zegoen lanean haren begikoa zen Francis William Astonekin batera, eta berari zor diogu esparru honetako ekarpenik handienetakoa. 2. irudian ikus daitezke garai hartako hastapenezko espektrometroetan lortzen ziren emaitzak. Orduan, parabola-espektometro esaten zitzaien horrelakoei. Plaka fotografikoan ikus daiteke nolako markak zeuden, masa/karga erlazioen arabera jarrita. Argi esan beharrekoa da termino hori atomoaren edo molekularen masa zati karga kopurua, besterik ez dela. Esaterako, CO+ ioirako 28 da zenbakia: 12-karbonoaren masa + 16-oxigenoaren masa zati bat. Hg2+ ioirako, 100 dugu zenbakia, atomo horren masa / 2 egiten delako. Jakingarri gisa esango dugu Th unitatea esleitu zitzaiola parametro horri, Thomsonen omenez. Hala ere, unitatea ez da nazio artean onartu, eta m/z gisa azaltzen da, Th eraren lilura bazter utzita.

Astonek ikusi zuen neoiaren (20 m/z) seinalearekin batera beste seinale txiki bat azaltzen zela (22 m/z). Zer ote zen hori? Zientzialari onak ziren eta hainbat saio eginda, hasiera mailako hipotesi batzuk baztertzen joan ziren: ez ziren ez CO2 molekulak (44/2 karga bikoiztunak), ez eta NeH2 molekulak. Gas noble hau aztertzen zen bakoitzean azaltzen zen seinale bitxi hura, bederatzi aldiz txikiagoa zena. Besterik ezin zen izan: bera ere neoia zen. 1913.ean, proposatu zuten neoia agian masa desberdinetako bi atomoz osatua egon litekeela: 20 eta 22 pisukoak, 9:1 proportzioan. Hori onartuta, erraz uler zitezkeen intentsitate desberdinetako seinaleak, bai eta 20,2 pisu atomiko ertaina (bi atomoen proportzioa kontuan hartuta). Astonek isotopo berri bat aurkitua zen.
“Isotopo” terminoa Frederick Soddyk sortu berria zen garai hartan, Margarett Toddek iradokita. Propietate berdinak baina masa ezberdinak dituzten atomoei erreferentzia egiteko asmatu zen terminoa. Egun, gauza arrunta iruditzen zaigu kontua, baldin eta kimika pixka bat jakinda kontuan hartzen badugu isotopoek neutroi kopuru desberdinak izan ditzaketela, baina garai hartan atomo azpiko partikula horiek aurkitu gabe zeuden artean! Gerra ostean, Astonek hobetu egin zuen bere tresna, eta lehenengo “masa-espektrometroak” garatu zituen (3. Irudia). Horrela, 212 isotopo natural aurkitu zituen. Kimika Nobel saria lortu zuen 1922. urtean. Soddyk aurreko urtean irabazia zuen saria.
Espektrometriaren hastapen garai horretan, Arthur Jefrrey Dempster goraipatu behar da. Berak, Chicagoko Unibertsitatean, sekzio magnetikoko lehenengo espektrometroak diseinatu zituen. Azken hauetan oinarrituta daude egungo tresna asko, eta haietan oinarrituta aurkitu zen 235-uranioa.

Gerrak, aurrerapenak eta hedadura
Hain zuzen ere 235-uranioa da espektrometria honen aplikazioen lehenengoetako baten eragile nagusia. Zoritxarrez. Manhattan egitasmoan ari zirelarik, Alfred Nierrek irauli egin zuen espektrometria. Izan ere, esparru horretako tresna berriak sortu zituen, Little Boy izenekoan erabilitako isotopoa islatzeko eta hobeto ezagutzeko. Ez litzateke ordea bidezkoa izango bere aurrerapenei eman zitzaien aplikazioagatik epaitzea. Zientzialari honek ulertu zuen masa-espektrometria honek garrantzi handia hartuko zuela, eta berez, musu-truk zabaldu zuen bere aurkikuntza beste esparru batzuetara: biologia (13-karbonoaren aberastea) edo geologia (lur-geruzaren isotopo bidezko datazioa).
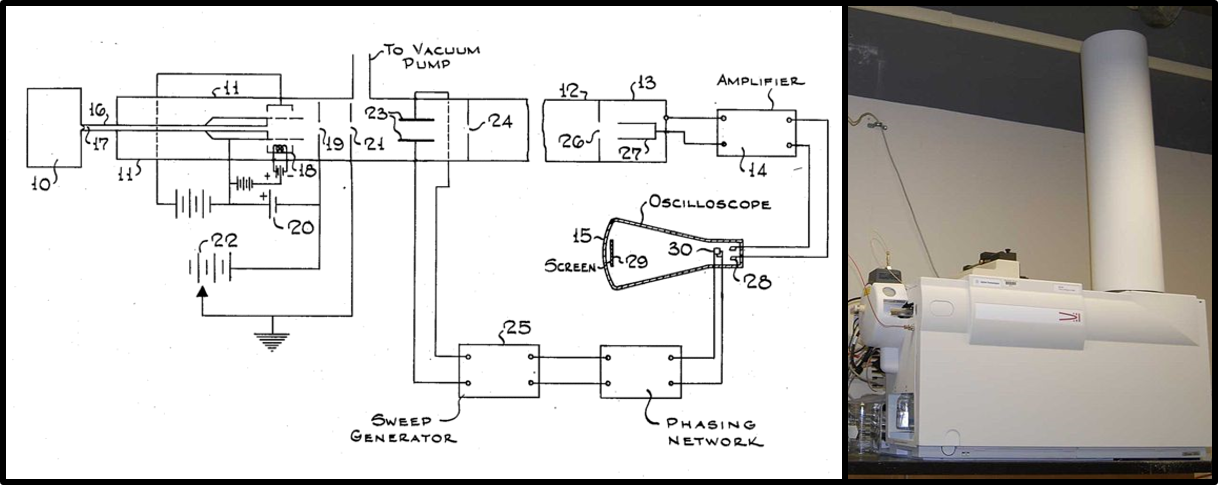
40 eta 50.eko hamarkadetan zehar hobekuntza handiak eginda, printzipio berrietan oinarritutako tresnak sortu ziren, ioiak banatzeko. Oso garrantzitsuak eta goraipatzekoak dira “hegaldi” motako tresnak”, W.E. Stephensek proposatuak. Honelakoetan, inpultso batek molekula ezberdinetan eragindako abiadura ezberdinen bidez banatzen dira molekulak. Sistema hau da hain zuzen irudikatzen errazena: zenbat eta astunagoak, hainbat eta beranduago iritsiko dira molekulak detektagailura. Aurrerapen handia izan zen era berean kuadripolo motako tresnak asmatzea. Horrelakoetan, zilindroak erabiltzen dira, korronte jarraituaren eta erradiofrekuentzien aldaketak eginez ioiak banandu ahal izateko. Izan ere, Wolfgang Paul eta Hans Georg Dehmeltek Fisikako Nobel saria lortu zuten 1989.ean, ioi-tranpagatik. Tranpa horretan garatu ziren aipatu printzipioak hiru dimentsiotan.
Joan gaitezen astiroago baina. Hasierako merkatuko espektrometroek ez zuten oso harrera onik izan. Hala gertatu zen neurri handi batean teknika oso ezezaguna zelako. Berez, aplikazio gehienak kuantitatiboak ziren, eta horrelakoa zen adibidez petrolio-findegian egiten den hidrokarburoen analisia. Hau da, konposatu jakin baten seinalea kontzentrazioarekiko proportzionala delarik, konposatuak lagin ezberdinetan zuen kontzentrazioa ezartzeko erabiltzen zen, eta horrela alferrik baztertzen zen masa-espektrometria metodoaren eskaintza onena: molekula ezezagunen identifikazioa.
Molekula baten izaera ezagutzeko, funtsezkoa da masa molekularra ezagutzea. Areago, molekula tresnan bertan zatikatu daiteke eta beraz, zatikien masa ere jakin daiteke, azkenean datu guztiak puzzle batean bezala uztartzeko. Hiru zientzialari ohartu ziren metodoaren aukera honetaz: Fred McLafferty, Klaus Biemann eta Carl Djerassi. Hala ere, Thomson izugarri aurreratu zitzaien beste guztiei, jadanik 1913.ean aurreikusi zuelako aplikazio hau. Edonola zientzialari hauei guztiei esker, Kimika Organikoaren arloan hedatu zen metodoa. Hasiera batean, alkaloideak eta esteroideak aurkitzeko erabili zen espektrometria hau. Izan ere, Djerassi pilula antisorgailua aurkitu zutenetako bat da. Horrela, erresonantzia magnetikoarekin batera, molekula berriak ezagutzeko metodo nagusia izatera iritsi zen masa-espektrometria.
Erabateko arrakasta
Espektrometria goraka zihoan, baina artean gainditzeko eragozpen handia zuen aurrean: nola lortu edozein molekula gas-ioi bihurtzea? Izan ere, oraindik masa-neurketaz baizik ez gara aritu, eta ez dugu bestelakorik jorratu. Gogoan izan behar dugu teknika honek masa/karga erlazioa neurtzen duela eta ezer gutxi lortuko dugula gure aztergaia ionizaturik ez badago. 60.eko hamarkadaren bukaera aurreko garaietan, metodoek ezin zituzten molekula ezlurrunkorrak erabili, edo batzuetan molekula erabat apurtzen zutelarik, galdu egiten zen masa molekularraren informazioa.
Gauzak horrela, biomolekulak ezin ziren aztertu, eta are gutxiago tamaina handiko proteinak. Aurrera egin behar zen eta bi ionizazio berri sortu ziren: Elektro-spray bidezko ionizazioa eta Matrizeak lagundutako Laser-Desortzioa/ionizazioa (ingelesez, MALDI). Horrela, hegoak jarri zitzaizkien “molekula elefanteei”. Hala esan zuen John B. Fennek Kimikako Nobel saria 2002.ean hartzean.

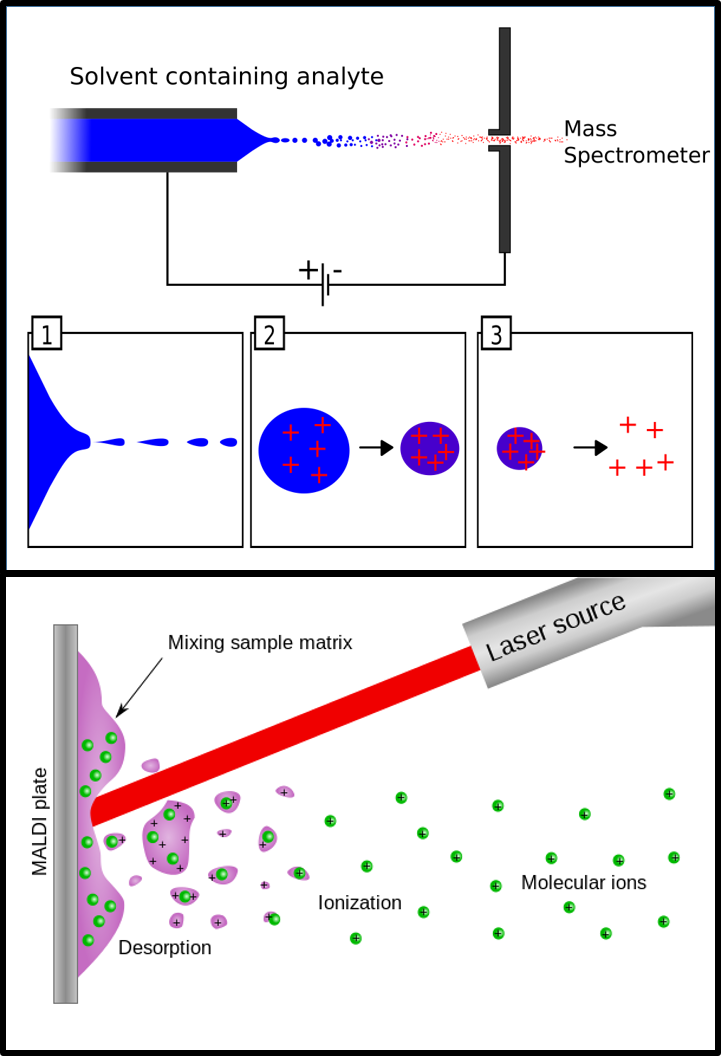
Fennek Koichi Tanaka japoniarrarekin partekatu zuen 2002.eko Nobel Saria, “makromolekula biologikoak analizatzeko ionizazio-metodo bigunen garapenagatik”. Lehenengoak ESI metodoa garatzegatik hartu zuen saria, baina esan beharrekoa da metodoa bera Malcom Dolek sortua zuela 1968.ean. Ionizazio metodo hau bakun samarra da: bere baitan lagina duen disolbatzaileak kapilar bat zeharkatzen du. Kapilar horri, molekulak ionizatzeko (karga positiboa edo negatiboa jartzeko) boltaje bat ezartzen zaio. Irtendakoan, likidoak aerosol bat sortuko du (spray bat), nebulizazio-gas baten laguntzaz. Disolbatzailea lurrintzen doan neurrian, tantak gero eta txikiagoak dira. Une jakin batean, tantak oso txikiak dira eta ondorioz, molekula kargatuen arteko aldaratze-indarra, azalezko tentsioa baino handiagoa da eta “leherketa” gertatzen da (6.irudia). Horrela, masa-analizagailura sartzeko moduko gas-ioiak lortzen dira.
Ionizazio mota honek aukera ematen du molekula anitz aztertzeko, bai eta 100.000 daltonetik gorako pisu molekularra duten molekulak aztertzeko ere. Gainera, oso abantailatsua da, disolbatzaile likidoak erabiltzen direlako, eta horrek posible egiten du metodo hau kromatografia likidoarekin elkartzea. Esan beharrekoa da banaketa-teknikarik arruntenetako bat dela kromatografia likidoa.
Bestetik, Tanakak oso metodo desberdina erabili zuen proteinak ionizatzeko: laser bat. Bere lorpena ukaezina da, baina eman zioten Nobel Saria nahiko eztabaidatua izan zen. Izan ere, batzuek pentsatzen dute Hillenkamp eta Karasi eman beharko zietela saria, zeren eta haiek garatu baitzuten egun egun MALDI modura ezagutzen duguna, eta teknika hau ez da Tanakaren metodo berbera. Eztabaida alde batera utzita, ez dugu oraindik esan MALDI ionizazio-metodoa zeharkakoa dela. Laser bidez erraz ionizatzen den matrize bat gehitzen zaio laginari, eta matrize hori da molekuletara bere karga transferitzen duena. Ionizazio-metodo hau oso ona da, batez ere aukera ematen duelako, animalia ehunak bezalako azalen irudiak egiteko.
XXI. mendean zehar, goraka joan dira masa-espektrometriaren aurrerapenak eta nagusi bilakatzen ari dira bereizmen handiko ekipoak (oso masa/karga erlazio antzekoak dituzten molekulak bereizten dituztenak). Horri begira gaudela, agian Orbitrap da azken urteotan egin izan den aurrerapen handiena: tranpa motako masa-espektrometroa, Fourier transformatua duena.
Baina aurrerantzean hitz egingo dugu espektrometriaren orainaz, teknika hau oso baliagarria suertatzen dela erakusten joango garelako hainbat esparrutan zehar.
Egilearen oharra: Masa atomikoa eta pisu atomikoa definitzeko era aldatzen joan da urteetan zehar. Esango dugu isotopo espezifiko baten masa dela masa atomikoa, eta elementuaren pisua atomikoa dela isotopo guztien masen batezbestekoa (aberastasuna kontuan hartuta).
Erreferentzia bibliografikoak
- Maher, Simon et al., (2015). Colloquium: 100 years of mass spectrometry: Perspectives and future trends. Reviews of Modern Physics, 87, 113-135. DOI: https://doi.org/10.1103/RevModPhys.87.113
- Griffiths, Jennifer et al., (2008). A Brief History of Mass Spectrometry. Analytical Chemistry, 80 (15), 5678-5683. DOI: 10.1021/ac8013065
- Borman, Stu et al., (2003). A Mass Spec Timeline. Today’s Chemist at Work, September, 47-49.
Egileaz: Oskar Gonzalez (@Oskar_KimikArte) UPV/EHUko Kimika Analitikoa Saileko ikertzailea da eta Zientzia eta Teknologia Fakultateko eta Arte Ederretako Fakultateko irakaslea ere.
Hizkuntza-begiralea: Juan Carlos Odriozola
Masa-espektrometriari buruzko artikulu-sorta
- Masa-espektrometria (I). Neoi isotopoetatik elefante hegalariengana
- A new hero is born: Masa-espektrometria justiziaren zerbitzura
- Nor dago icebergaren alden ezkutuan?
- Konposatu galduren bila
- Metabolomika: osotasuna, zatien baturaren aurrean
- Esploratu gabe dauden lurraldeak kartografiatzen: masa-espektrometria bidezko irudia
- Proteomika: Proteinak eta Masa Espektrometria eskutik helduta
10 iruzkinak
[…] Masa-espektrometria (I). Neoi isotopoetatik elefante hegalariengana […]
[…] garrantzitsuak plazaratuko dira Zientzia Kaieran eta Cuaderno de Cultura Científica blogetan. Gaurkoan masa-espektrometria teknikari buruz hitz egin dute. Egungo analisi-teknika moldakorrena eta ahaltsuena da; aukera ematen du oso kantitate txikietan […]
[…] Masa-espektrometria izeneko analisi teknikak laguntzen gaitu atomoen zein molekulen hatz-marka identifikatzen. Hatz-marka hori lortzeko masa-espektrometroak gas-fasean dauden atomo/molekula ionizatuen masa/karga (m/z) erlazioak neurtzen ditu. Masa-espektrotik atomoen zein molekulen masa zehatza ezagutu daiteke, isotopoen presentzia determinatu eta, molekulen kasuan, apurketa […]
[…] Masa-espektrometria izeneko analisi teknikak laguntzen gaitu atomoen zein molekulen hatz-marka identifikatzen. Hatz-marka hori lortzeko masa-espektrometroak gas-fasean dauden atomo/molekula ionizatuen masa/karga (m/z) erlazioak neurtzen ditu. Masa-espektrotik atomoen zein molekulen masa zehatza ezagutu daiteke, isotopoen presentzia determinatu eta, molekulen kasuan, apurketa […]
[…] bat erabili genuen, analisi-modu gidatuarekin ikusi ezin genituen konposatuak aurkitu ahal izateko masa-espektrometriaren […]
[…] telesailek laborategi zientifikoa ekarri dute gure bizitzara eta, harekin batera, baita masa-espektrometria ere. Errealitatean eta fikzioan gertatzen dena ez da guztiz berdina, baina bi kasuetan ere oso […]
[…] metabolomikaren hasieran erresonantzia magnetiko nuklearra (RMN) erabiltzen zen batez ere. Baina masa-espektrometrian (MS) oinarritutako metabolomikaren ospea areagotzen joan da denborarekin. Ebazpen handiko tresnak […]
[…] Masa-espektrometria (I). Neoi isotopoetatik elefante hegalariengana […]
[…] eta proteina zatikiak (peptidoak) bezalako makromolekulak ionizatzea eta gas fasera aldatzea elefanteak hegaz egitea hainako egitekotzat jo zen luzaroan. Ionizazio “arina” izena eman zitzaien bi […]
[…] legez kanpoko zura. Gaitz honi aurre egiteko teknika berritzaileak erabiltzen dira, hala nola masa-espektrometria edota isotopoen analisia, bai eta gene-teknikak ere zur-trafikoa ikertzeko erabiltzen dira […]