RNA mezularian oinarritutako txertoak, bularreko minbiziaren aurka
RNA mezularian oinarritutako txertoek berebiziko garrantzia izan zuten SARS-Cov-2 birusak eragindako pandemiari aurre egiteko, eta etorkizuneko beste gaixotasun batzuen aurkako estrategia eraginkor moduan aurkeztu ziren. Orain, BioNTech enpresa alemaniarrak —COVID-19aren aurkako txertoetariko bat garatu zuenak— aurkeztu berri ditu bularreko minbizi hirukoitz negatiboari aurre egin dakiokeen entsegu kliniko bateko lehenengo faseko emaitza itxaropentsu batzuk.
Bularreko minbizi hirukoitz negatiboa (ingelesez TNBC, triple-negative breast cancer) bularreko minbizien artean agresiboenetarikoa da, eta, hazkuntza azkarra izateaz gain, sarri berragertzen den horietarikoa. Bularreko minbizien % 10-20 bitartean dira hirukoitz negatiboak, eta horrela deitzen dira minbizi-zelulek pairatutako mutazioen ondorioz ez dutelako adierazten progesterona eta estrogeno hartzailerik, ezta HER2 proteinarik ere. Tratatu ondoren ohikoak izaten dira berragerpenak eta metastasiak; gainera, gaur egun klinikan erabiltzen diren estrategia gehienak antzuak dira tumoreak berriro hazten direnean.
BioNTech enpresa bioteknologikoa ezaguna egin zen COVID-19 gaixotasunak eragin zuen pandemia-garaian haiek izan zirelako txerto eraginkorrenetariko bat sortu zuten enpresetako bat. COVID-19ari aurre egiteko txertoa RNA mezularian (RNAm) oinarrituta dago. Gure zelulek proteinak sortzeko informazioa nukleoan gordetzen dute DNA moduan —geneetan—, eta, zelulek behar bat dutenean, nukleoan bertan DNA RNAm bihurtzen dute transkripzio izeneko prozesu baten bidez. RNAm-a nukleotik irten eta zitoplasmako erribosometan proteinak sortzeko erabiltzen da, itzulpen izeneko prozesuaren bidez. COVID-19aren aurkako txertoaren kasuan, SARS-CoV-2 birusaren proteina baten zati bat kodetzen duen RNAm-a gure gorputzean sartzen da nanopartikula batzuen barruan. Gure gorputzeko zelulek nanopartikularen edukia barneratzen dute RNAm moduan, eta proteina zati hori sortzen dute. Proteina arrotza denez, sistema immuneko zelulek ezagutu eta erantzuna prestatzen dute, etorkizunean birusarekin bat egiten badute hari aurre egiteko. Antzerako estrategia erabili dute BioNTech-ekoek bularreko minbiziari aurre egiteko.
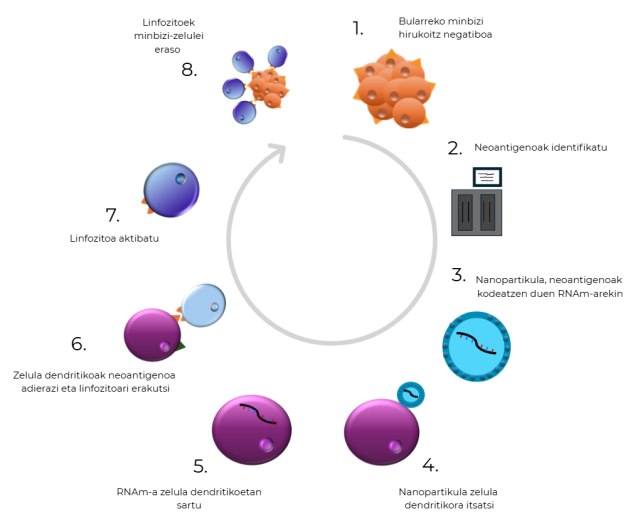
Kasu honetan, paziente bakoitzaren tumoreak analizatu dira sekuentziazio bidez, eta tumoreek azaltzen dituzten neoantigenoak identifikatu dira (eskemako 2. puntua). Neoantigenoak dira tumore-zeluletan mutazioen ondorioz sortzen diren antigeno espezifikoak; hau da, erantzun immunea sortu dezaketen proteinak. Berezitasun bat dute: nahiz eta tumoreak giza gorputzeko zelula eraldatuak izan, neoantigenoak ez dira agertzen zelula osasuntsuetan. Horregatik dira hain baliagarriak neoantigenoak. Neoantigeno horiek espezifikoak dira paziente bakoitzaren arabera, eta txerto jakin bat sortuko da gaixo bakoitzarentzat bakoitzak duen neoantigenoetan oinarrituta. Behin neoantigenoak identifikatuta, RNAm moduan sartzen dira nanopartikuletan (eskemako 3. puntua). Nanopartikulak gure gorputzeko zelula dendritikoetara bideratzen dira (eskemako 4. puntua). Zelula dendritikoak sistema immuneko zelula bitartekariak dira. Antigenoak barneratu eta linfozitoei erakusteko gaitasuna dute, eta, horrela, linfozitoak erantzun immune zuzena eragiteko trebatzen dira. Zelula dendritikoek, nanopartikulek daramaten RNAm-a barneratzean (eskemako 5. puntua), RNAm-a hori proteina bihurtzen dute haien zitoplasman; kasu honetan, neoantigenoak sortzen dituzte. Zelula dendritikoek neoantigenoak zitoplasman sortu ondoren mintzean adierazten dituzte, eta linfozitoei erakusten dizkiete (eskemako 6. puntua). Linfozitoak neoantigenoak ikusi ondoren trebatu egiten dira (eskemako 7. puntua), eta, horrela, neoantigeno hori daramaten zelulen aurka jotzen dute (eskemako 8. puntua); kasu honetan, bularreko minbizi-zelulen aurka.
Entsegu honetan, 14 paziente tratatu ziren estrategia hori erabiliz. Guztiak bularreko minbizi hirukoitz negatiboak ziren; hasierako tratamendua jaso ondoren, txertatu egin ziren etorkizuneko berragertzeak eta metastasiak saihesteko. 14 kasutatik 10 bizirik daude sei urte beranduago, eta ikusi da epe motzeko zein epe luzeko erantzunak eragiten dituzten linfozito azpimota asko agertzen dituztela. Egiari zor, 14 paziente ez da kopuru handia ondorio sendoak ateratzeko, baina esan dezakegu txertoaren eraginkortasuna frogatu dela; orain, paziente gehiagorekin frogatu beharko da, sakonago aztertzeko eta etorkizuneko tratamendu moduan erabili ahal izateko.
Erreferentzia bibliografikoa:
Sahin, U.; Schmidt, M.; Derhovanessian, E.; Cortini, A.; Vogler, I.; Omokoko, T.; Godehardt, E.; Attig, S.; Newrzela, S.; Grützner, J.; Bidmon, N.; Bolte, S.; Brachtendorf, S.; Stuhlmann, T.; Langer, D.; Brüne, D.; Blake, J.; Feldner, A.; Lindman, H.; Schneeweiss, A.; Eichbaum, M.; Türeci, Ö. (2026). Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature, 651, 1088-1096. DOI: 10.1038/s41586-025-10004-2
Egileaz:
Iker Badiola Etxaburu (@ikerbadiola.bsky.social) EHUko Medikuntza eta Erizaintza Fakultateko irakaslea eta EHUko Kultura Zientifikoko Katedrako zuzendaria da.